
Лабораторные тесты, подтверждающие действие вакцины
Определение цитокинов подтверждает включение клеточного
иммунного ответа после введения вакцины
Под действием РЕСАН происходит активация клеток системы иммунитета. На Рис. 1 изображена классическая схема функционирования Т-хелперов.
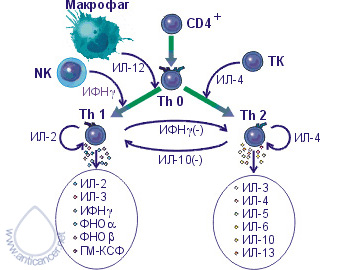
Рис. 1. Развитие и взаимодействие Т-хелперов 1 и 2 типов,
продукция цитокинов
Преобладающее образование Т-хелперов 1 типа (Th1) указывает на усиление клеточного иммунного ответа, а преобладающее образование Т-хелперов 2 типа (Th2) – на усиление гуморального иммунного ответа. По содержанию цитокинов в сыворотке крови делают заключение о преимущественном включении клеточного или гуморального иммунного ответа. После введения вакцины РЕСАН происходит достоверное повышение уровня ФНО-a (фактора некроза опухоли альфа) и ИФН-g (гамма-интерферона), указывающее на активацию клеточного иммунного ответа. Определение этих цитокинов в сыворотке крови проводят до введения препарата и через 7-14 суток после введения. В норме содержание ФНО-a и ИФН-g в сыворотке крови составляет 0-50 пг/мл.
Тест розеткообразования, подтверждающий противоопухолевое
действие препарата
Производится забор крови как для оценки иммунного статуса. Тест проводят до введения препарата и через 10-12 дней после введения.
Необходимо в стерильных условиях из опухолевой ткани, полученной при биопсии, вырастить культуру опухолевых клеток. Готовят суспензию опухолевых клеток 6x107 в 1 мл. Из плазмы крови готовят суспензию лейкоцитов 2x106 в 1 мл. В круглодонные лунки иммунопланшета вносят по 0,1 мл суспензий лейкоцитов и опухолевых клеток, перемешивают. Инкубируют 30 минут при 37°С. Центрифугируют 3 минуты при 1000 об/мин. Надосадочную жидкость отсасывают, добавляют 0,1 мл 0,05% раствора глютарового альдегида, аккуратно перемешивают. Берут 0,1 мл суспензии клеток и наносят на предметное стекло. Высушивают, фиксируют спиртом и окрашивают по Романовскому-Гимза.
Подсчитывают розетки при микроскопии. Увеличение розеткообразования лимфоцитов с опухолевыми клетками указывает на формирование противоопухолевого иммунитета.
Тест лизиса опухолевых клеток (стерильные условия)
Из опухолевой ткани, полученной при биопсии, необходимо вырастить культуру опухолевых клеток. Тест проводят до введения препарата и через 10-12 дней после введения.
Из культуры опухолевых клеток готовят суспензию 2,5·103 клеток в 1 мл. В лунки микропланшета (Falcon № 3034, США) вносят 20 мкл этой суспензии. Через 24 часа из плазмы крови готовят суспензию Т-лимфоцитов 5·105 клеток в 1 мл. Из лунки микропланшета отсасывают надосадочную жидкость, около 200 опухолевых клеток остаются адгезированными к поверхности лунки. К ним добавляют 20 мкл суспензии Т-лимфоцитов, инкубируют в атмосфере с 10% CO2 в течение 48 часов. После двукратной отмывки фиксируют препарат спиртом и окрашивают раствором Гимза. Подсчитывают количество оставшихся в живых опухолевых клеток. Результат оценивают по формуле лизиса опухолевых клеток (ЛОК) в %, она показывает % лизированных за 48 часов опухолевых клеток.
ЛОК=(ОККОН-ОКОП)/ОККОН·100%,
где ОККОН – количество опухолевых клеток в контроле, ОКОП – количество опухолевых клеток в опыте. Если ЛОК=30% и более, значит, противоопухолевый иммунитет сформировался.
Сравнение проводим с результатами до введения препарата.
Мониторинг эффективности иммунотерапии по уровню
опухольассоциированных антигенов
Для оценки эффективности иммунотерапии можно использовать мониторинг опухольассоциированных антигенов.
- Сохранение динамики роста опухольассоциированных антигенов в крови больных указывает на отсутствие эффекта от иммунотерапии.
- Замедление динамики роста опухольассоциированных антигенов указывает на включение иммунного ответа недостаточной силы
- Остановка роста или снижение уровня опухольассоциированных антигенов говорит об эффективном включении противоопухолевого иммунного ответа.
|
Опухолевый маркер
|
|
CA M29, CA27.29, MUC-1, TPS, BCA225, 317G5, 454C11, MCA, Ferritin, neopterin, IGF-I (у женщин в пременопаузе) |
|
Повышенная концентрация неоптерина в сыворотке крови человека является новым полезным маркёром активации клеточного иммунитета. Увеличение уровня неоптерина при различных инфекциях и опухолях предшествует появлению специфических антител в сыворотке крови.




